بحث عن تكوين الايون

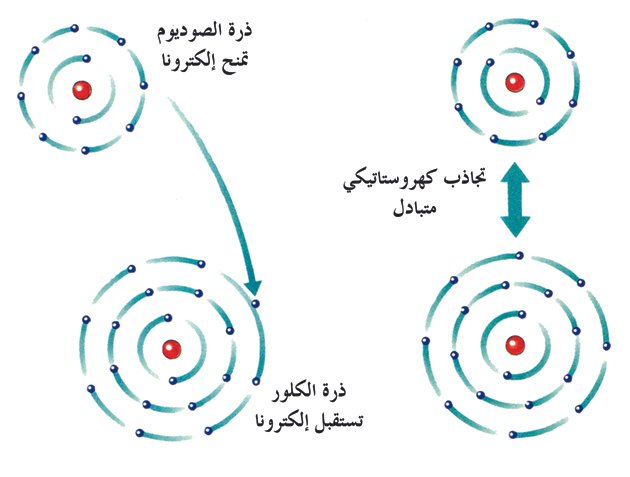
2 يكتسب اللامعدن اللافلز هذا الإلكترون ويصبح سالب الشحنة.
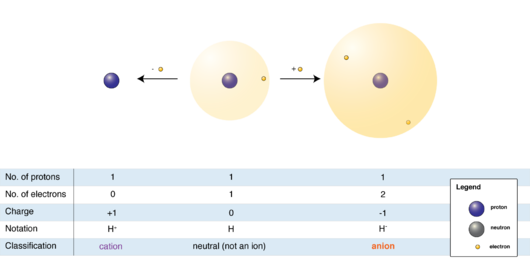
بحث عن تكوين الايون. أسماء المركبات الكيميائية وصيغها. الأيون عبارة عن ذرة أو جزيء يحمل شحنة كهربائية ويكون هذا عن طريق إما إكتساب إلكترونات فيكون عدد الإلكترونات أكبر من عدد البروتونات وبالتالي يتكون أيون سالب الشحنة أو يفقد الجزئ أو الذرة الإلكترونات وبالتالي يكون عدد البروتونات أكبر من عدد الإلكترونات وبالتالي يتكون أيون موجب. الايون الموجب ذرة غير متعادلة كهربائي ا ذات شحنة موجبة حيث عدد البروتونات فيها أكبر من عدد الإلكترونات أي أن الشحنة الموجبة في الذرة أعلى من الشحنة السالبة. تتكون الرابطة الأيونية من ثلاث خطوات.
تعرف المركبات الأيوني ة بأنها مركبات تنتج عن تفاعل عنصر فلزي يتألف من ذرات تميل إلى فقد الإلكترونات بسهولة مع عنصر آخر لا فلزي يميل إلى اكتساب الالكترونات بسهولة بحيث يتم نقل الإلكترونات لإنتاج الأيونات ويتم تحقيق الاستقرار للمركب الأيوني بواسطة قوى الجذب الكهروستاتيكية وهي الروابط الأيوني ة. يمكن التمييز بين الأيونات السالبة وبين الأيونات الموجبة. المركبات العضوية ومجموعاتها الوظيفية. بحث عن تكون الأيون.
بحث حول العناصر والمركبات. الأ ي ون أو الشاردة ملاحظة 1 هو نوع كيميائي ذر ة أو جزيء مشحون كهربائيا. 1 يفقد المعدن الفلز النشط الإلكترون الأكثر بعدا عن النواة ويصبح موجب الشحنة. تتكو ن الأيونات السالبة anion بعكس الطريقة التي تتكون فيها الأيونات الموجبة فهي تتكون عن طريق اكتساب العناصر اللافلزية للإلكترونات بدلا من فقدانها وذلك لأن مستوى الطاقة الخارجي لهذه العناصر ممتلئ تقريبا ومن الجدير بالذكر أن العناصر التي تكون على يمين الجدول الدوري تمتلك ألفة إلكترونية بالإنجليزية.
تتشكل الأيونات عندما تقوم الذرة إم ا بفقدان أو اكتساب إلكترون وذلك لتصل إلى توزيع إلكتروني شبيه بذلك الموجود في الغازات النبيلة وذلك للوصول إلى وضع طاقة أعلى وتختلف الذرات في كونها تقوم بكسب أو فقد الإلكترونات بناء على تركيبها حيث تقوم المعادن بخسارة الإلكترونات مم ا يجعلها أيونات موجبة مقابل المواد غير المعدنية التي تكتسب الإلكترونات وبالتالي تصبح سالبة الشحنة. Electron affinity أكبر من العناصر التي تكون على يسار الجدول الدوري وذلك لأن مستويات الطاقة تكون ممتلئة تقريبا بالإلكترونات.